Curvas de Presión de Vapor Diagramas de Fases para la Vaporización
Diagramas de Fases para Curvas de Presión de Vapor
Aunque los diagramas de fases se utilizan principalmente por los químicos y en el entorno de laboratorios, estas herramientas son sorprendentemente útiles para ingenieros mecánicos y directores de planta encargados de análisis de muestras. En algunos sistemas analíticos, las muestras líquidas deben ser convertidas en gas mediante la vaporización para poder analizarlas. El proceso de vaporización es esencialmente un equilibrio entre las variables temperatura, presión y caudal – y las curvas de presión de vapor de un diagrama de fases permiten a los ingenieros identificar los cambios de fase de distintos materiales y compuestos químicos. Es fundamental comprender la relación entre la presión de vapor y el diagrama de fases.
Nuestros centros locales de ventas y servicio tienen especialistas que pueden ayudarles.
Cómo Leer una Curva de Presión de Vapor
Por ejemplo, vamos a aplicar una mezcla de gas hipotética de pentano con un 20% de hexano como un diagrama de fase completo (ver el gráfico de presión de vapor de abajo). Cuando la muestra está por encima del punto de ebullición (línea azul), toda ella está en fase líquida. La muestra debe estar en estado líquido cuando entra en el vaporizador. Cuando la muestra está por debajo de su punto de rocío (línea dorada), toda ella es vapor. La muestra debe ser toda vapor cuando sale del vaporizador.
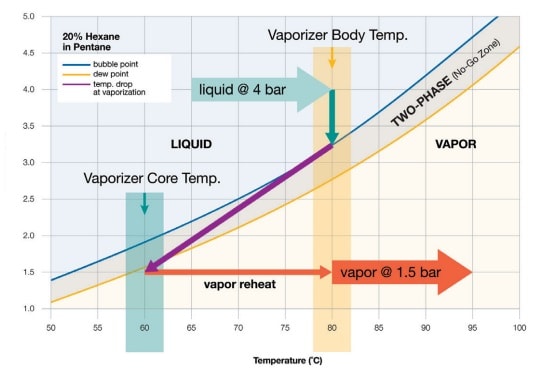
Entre las líneas del punto de ebullición y punto de rocío, está la “zona de exclusión.” Esta zona representa el rango de ebullición de la muestra. Aquí, la mezcla está en dos fases: parte líquida y parte vapor. Cuando la mezcla cae en la zona de exclusión, se fracciona y ya no es adecuada para el análisis. El objetivo de la vaporización es ajustar la temperatura, caudal y presión de forma que la muestra pase instantáneamente del lado líquido al lado vapor de la zona de exclusión. En el caso de las muestras puras o casi puras, hay muy poco o ningún rango de ebullición o zona de exclusión. Las líneas del punto de ebullición y del punto de rocío están una sobre la otra o prácticamente juntas.
Las muestras puras o casi puras se convertirán en vapor con la misma composición, tanto si se evaporan como si se vaporizan. Algunas muestras industriales se acercan a este nivel de pureza y se convierten bastante fácilmente. Pero también hay otras que tienen un rango de ebullición o zona de exclusión tan amplia que no pueden ser vaporizadas satisfactoriamente. No hay forma que la muestra pase del lado al lado de vapor evitando la zona de exclusión. En estos casos las variables no se pueden manipular para evitar el fraccionamiento.
En el diagrama de presión de vapor de arriba, la banda entre los puntos de ebullición y de rocío es lo suficientemente estrecha como para que con los ajustes adecuados la muestra pase eficientemente del lado líquido al lado vapor de la zona de exclusión. Pero al mismo tiempo es demasiado ancha como para permitirse ser imprudente.
Ajustar los Parámetros de Temperatura, Presión y Caudal para los Procesos de Vaporización
Siguiendo con el ejemplo del diagrama (20 % de hexano en pentano), es necesario ajustar con precisión los parámetros de control de temperatura, presión y caudal para garantizar el éxito del proceso de vaporización, según lo indicado en la curva de presión de vapor. En general, en la entrada se necesitan alta presión y baja temperatura. Contrariamente, en la salida se necesitan alta temperatura y baja presión. Hay límites en cuanto a los máximos y mínimos de esos parámetros, y no todas las restricciones se pueden controlar.
-
Calcule la Presión de Entrada para su Vaporizador
La presión de entrada, que es fija, es la presión de proceso—la que le llega al vaporizador ubicado cerca de la válvula de entrada En el diagrama de ejemplo, esa presión es de 4 bar. La presión alta es mejor porque permite al vaporizador mantener alta la temperatura sin alcanzar el punto de ebullición del líquido que llega.
-
Ajuste la Temperatura de Entrada para una Vaporización Completa
Ajustar la temperatura de entrada tiene dos objetivos. El primero, la temperatura debe ser suficientemente baja como para que cuando la muestra entre en el vaporizador, sea totalmente líquida. En el diagrama de ejemplo, el punto de ebullición a 4 bar es 88°C. Con el objetivo de evitar el fraccionamiento, es mejor elegir un número redondo y suficientemente alejado de 88°C para evitar la zona de exclusión. Un ejemplo de temperatura segura sería 80°C.
El segundo objetivo es mantener la temperatura lo suficientemente alta como para favorecer el flash completo de la muestra—asegurando que lo que salga del vaporizador sea solo vapor. Cuando se vaporiza la muestra, la temperatura cae de acuerdo a las leyes de la conservación de la energía. La temperatura inicial de la muestra debe ser suficientemente alta como para que tras la caída de presión ésta no vaya al intervalo de ebullición. En el diagrama del ejemplo, la temperatura del vapor tras la caída de presión es de 60°C—justo en el lado vapor de la línea del punto de rocío.
-
Ajuste la Presión de Salida para una Vaporización Adecuada de la Muestra
Al ajustar la presión de salida, el objetivo es disminuir la presión por debajo de la línea del punto de rocío. En el diagrama del ejemplo, la presión de salida esta a ajustada a 1,5 bar. Si la presión de salida fuese ligeramente superior, la muestra no se vaporizaría por completo y se fraccionaría.
-
Controle el Caudal con Válvulas y Medidores de Caudal
El caudal se ajusta aguas abajo en una válvula y un rotámetro, no en el vaporizador. En un sistema de toma de muestras es deseable un alto caudal de vapor porque transporta la muestra hacia el analizador más rápido. Pero un alto caudal puede ser problemático también, porque hace falta más calor para vaporizar la muestra. O lo que es lo mismo, el alto caudal provoca una mayor bajada de temperatura en el momento de la vaporización. En el diagrama del ejemplo, la línea púrpura muestra la bajada de temperatura. Según aumenta el caudal, la temperatura aumenta considerablemente.
Otra variable que influye en la caída de temperatura es la capacidad de transferir calor del vaporizador. La construcción de algunos vaporizadores permite una transferencia de calor más eficiente a la muestra. Cuando una muestra líquida se convierte en vapor y su temperatura baja, se equilibra aprovechando el calor del acero inoxidable a su alrededor. La cuestión crítica es la eficiencia con la que el vaporizador puede volver a calentar y mantener caliente la muestra. Cuanto más calor pueda utilizar la muestra menor es la bajada de temperatura durante la vaporización. Hasta es posible que el vaporizador esté caliente al tacto en el exterior pero frío en el núcleo. Eso se da porque la muestra vaporizada atrae mucha cantidad de calor y el vaporizador no puede transferir suficiente calor para continuar. La mejor solución es reducir el caudal.
En resumen, la bajada de temperatura observada en el diagrama de presión de vapor es producto del caudal y de la capacidad de transferencia de calor del vaporizador. Con un vaporizador de buena calidad y un bajo caudal, la línea del diagrama sería más vertical. Desafortunadamente, no existe una forma fácil de calcular la ubicación precisa de la caída de temperatura dentro de un diagrama de fases. Esta relación específica entre la presión de vapor y el diagrama de fases no puede generarse con ningún programa de software conocido. Por tanto, el proceso de vaporización implica algún tipo de aproximación. Como norma general, mantenga el caudal lo más bajo posible sin producir un retardo inaceptable en el trayecto de la muestra al analizador. Es mejor empezar con un bajo caudal y ensayar incrementos que empezar con una tasa de caudal mayor.
Para obtener asistencia sobre las mejores prácticas en relación a las curvas de presión de vapor utilizando los diagramas de fases para los sistemas de toma de muestra, contacte con su centro local de ventas y servicio Swagelok.
Artículos sobre el Proceso de Toma de Muestras y Vaporización
Cómo Ubicar las Boquillas de picaje en un Sistema de Toma de Muestras Líquidas y de Gas Natural
Los detalles pueden ser toda la diferencia de un sistema de toma de muestras eficiente. Evite retardos en los análisis, contaminación de muestras y resultados imprecisos en sus sistemas de toma de muestras líquidas o gaseosas, poniendo en práctica las sugerencias del experto en instrumentación analítica de Swagelok, Karim Mahraz.

5 Revelaciones Comunes sobre los Sistemas de Analizadores de Procesos en 50 años de Formación
Posiblemente los sistemas de toma de muestras sean algunos de los sistemas más desafiantes de planta en relación a su diseño y operación. El veterano de la industria e instructor industrial Tony Waters, comparte los descubrimientos más importantes de sus alumnos durante los últimos 50 años.

10 Consejos para Mejorar los Sistemas de Muestreo
Gestionar una operación de instrumentación analítica no es nada fácil. Obtener resultados consistentes puede ser una lucha hasta para los ingenieros más experimentados. Afortunadamente, hay bastantes consejos sencillos que su equipo puede utilizar para mejorar su sistema de toma de muestras.

