Courbes de pression de vapeur : gérer la vaporisation avec les diagrammes de phases
Diagramme de phases et courbes de pression de vapeur
Bien que les diagrammes de phases soient principalement utilisés par les chimistes en laboratoire, ces outils sont étonnamment utiles à des ingénieurs ou à des directeurs d’installation chargés d’analyser des échantillons. Dans certains systèmes d’analyse, un échantillon liquide doit impérativement être transformé en gaz par vaporisation avant qu’il ne puisse être analysé. Le processus de vaporisation nécessite un équilibre entre les variables de température, de pression et de débit – or, les courbes de pression de vapeur d’un diagramme de phases renseignent sur les changements d’état de divers matériaux et composés chimiques. Il est essentiel de bien comprendre la relation entre diagramme de phases et pression de vapeur.
Vous trouverez localement des spécialistes capables de vous aider dans nos centres de vente et de services.
Comment lire un diagramme de phases
Nous prendrons comme exemple le diagramme de phases d’un mélange gazeux d’hexane et de pentane contenant 20 % d’hexane (voir le graphique ci-dessous). Lorsque l’échantillon se trouve au-dessus de la courbe de bulle (ligne bleue), il se trouve entièrement à l’état liquide. Un échantillon doit être dans cet état à son entrée dans le vaporiseur. Lorsque l’échantillon se situe au-dessous de la courbe de rosée (ligne orange), il se trouve entièrement à l’état gazeux. Un échantillon doit être dans cet état à sa sortie du vaporiseur.
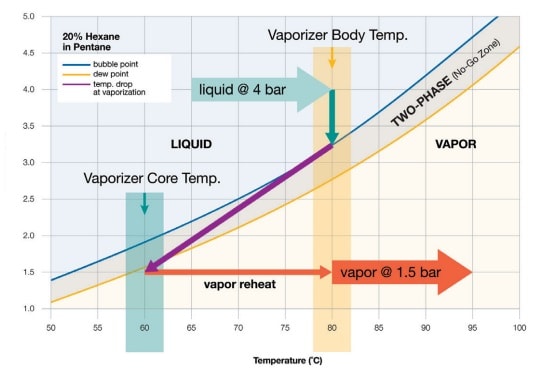
Entre les courbes de bulle et de rosée se trouve la « zone interdite ». Cette zone correspond au domaine d’ébullition de l’échantillon. Ici, deux phases cohabitent, le mélange étant partiellement à l’état liquide et partiellement à l’état gazeux. Si l’échantillon reste dans la zone interdite, il se fractionne et ne peut plus être utilisé pour une analyse. L’objectif est de régler la température, le débit et la pression de sorte que l’échantillon passe immédiatement du côté liquide au côté vapeur de la zone interdite. Avec des échantillons purs ou presque purs, le domaine d’ébullition ou zone interdite est réduit, voire inexistant. Les courbes de bulle et de rosée sont simplement superposées ou presque.
Les échantillons liquides purs ou presque purs se transforment en un gaz ayant la même composition, que ce soit par évaporation ou par vaporisation. Certains échantillons industriels approchent ce niveau de pureté et se transforment relativement facilement en vapeur. Par contre, certains échantillons ont un domaine d’ébullition tellement étendu qu’il est impossible de les vaporiser correctement. Pour de tels échantillons, il n’existe pas de moyen pour passer de la phase liquide à la phase vapeur en évitant la zone interdite. Dans ce cas, il est impossible de jouer sur les variables pour éviter leur fractionnement.
Sur le graphique représenté ci-dessous, la bande située entre les courbes de bulle et de rosée est assez étroite pour que l’échantillon puisse, avec des réglages appropriés, passer effectivement du côté liquide au côté vapeur sans passer par la zone interdite. Cela dit, cette même bande est suffisamment large pour que l’on se dispense de prendre certaines précautions.
Régler les paramètres de température, de pression et de débit pour le processus de vaporisation
Continuons avec le même mélange d’hexane et de pentane. Les paramètres de température, de pression et de débit doivent être réglés avec soin en s’appuyant sur le diagramme de phases pour assurer un processus de vaporisation réussi. D’une manière générale, une pression élevée et une température basse sont nécessaires à l’entrée du vaporiseur. À l’inverse, une température élevée et une pression basse sont nécessaires à la sortie. Ces paramètres doivent toutefois rester dans certaines limites et il n’est pas possible de maîtriser toutes les contraintes.
-
Calculer la pression à l’entrée du vaporisateur
La pression à l’entrée du vaporiseur, qui est fixe, est celle du process, à condition que le vaporiseur soit proche de la vanne de prélèvement. Sur le diagramme donné en exemple, cette pression est de 4 bar. Une pression élevée est préférable, car elle permet au vaporiseur de maintenir une température élevée sans provoquer l’ébullition du liquide entrant.
-
Régler la température à l’entrée du vaporiseur pour obtenir une vaporisation complète
La température à l’entrée du vaporiseur doit être réglée en poursuivant deux objectifs. Tout d’abord, la température doit être assez basse pour que l’échantillon soit entièrement liquide lorsqu’il pénètre dans le vaporiseur. Sur le diagramme donné en exemple, la température d’ébullition à 4 bar est de 88°C. Pour empêcher le fractionnement de l’échantillon, il est préférable de choisir un nombre entier relativement éloigné de 88° afin d’éviter la zone interdite. On pourra raisonnablement opter pour une température de 80°C.
Ensuite, la température doit rester suffisamment élevée pour entraîner la vaporisation instantanée et complète de l’échantillon, et garantir ainsi que seule de la vapeur sort du vaporiseur. Lors de la vaporisation, la température de l’échantillon chute, conformément à la loi de conservation de l’énergie. La température de l’échantillon doit être assez élevée au début pour que l’échantillon ne se retrouve pas dans la zone interdite après la chute de pression. Sur le diagramme donné en exemple, la température de la vapeur après la chute de pression est de 60°C, juste au-delà de la courbe de rosée, côté vapeur.
-
Régler la pression à la sortie de manière à obtenir une vaporisation adéquate de l’échantillon
Lorsque l’on veut régler la pression à la sortie du vaporiseur, l’objectif est d’abaisser la pression en dessous de la courbe de rosée. Dans le diagramme donné en exemple, la pression de sortie est réglée à 1,5 bar. Si la pression de sortie était à peine supérieure, l’échantillon ne se vaporiserait pas entièrement et se fractionnerait.
-
Contrôler le débit avec des vannes et des rotamètres
Le débit est réglé en aval à l’aide d’une vanne et d’un rotamètre, et non pas au niveau du vaporiseur. Dans un système d’échantillonnage, il est souhaitable d’avoir un débit de vapeur élevé, car cela permet un déplacement plus rapide de l'échantillon vers l’analyseur. Toutefois, un débit élevé peut être un problème, car la vaporisation de l’échantillon nécessite alors plus de chaleur. Autrement dit, un débit élevé entraîne une chute de température plus importante au moment de la vaporisation. Sur le diagramme donné en exemple, la flèche violette représente la chute de température. Lorsque le débit augmente, la température chute fortement.
Une autre variable qui influence la chute de température est la capacité du vaporiseur à transférer la chaleur. Certains vaporiseurs sont fabriqués de telle façon que les transferts de chaleur à l’échantillon se font plus efficacement. Lorsque l’échantillon liquide se transforme en vapeur et que sa température chute, il tire de la chaleur de l’acier inoxydable qui l’entoure. La question essentielle est de savoir jusqu’à quel point le vaporiseur peut remplacer la chaleur et continuer à la transférer à l’échantillon. Plus l’échantillon parvient à absorber de la chaleur, moins sa température chute pendant la vaporisation. Dans certains cas, il est possible que le vaporiseur soit chaud au toucher à l’extérieur tout en étant froid à l’intérieur. L’échantillon vaporisé absorbant de grandes quantités de chaleur, le vaporiseur ne parvient alors plus à transférer suffisamment d’énergie pour faire face à cette absorption. La meilleure solution consiste à diminuer le débit.
En résumé, la chute de température visualisée sur le diagramme de phases dépend du débit de l’échantillon et de la capacité du vaporiseur à transférer la chaleur. Avec un vaporiseur de bonne qualité et un débit faible, la flèche tendra vers la verticale. Malheureusement, il n’existe pas de moyen simple pour calculer l’emplacement précis de la flèche violette (chute de température) sur un diagramme de phases. Aucun logiciel connu ne permet de générer cette relation spécifique entre pression de vapeur et diagramme de phases. Par conséquent, le processus de vaporisation implique une certaine approximation. En règle générale, maintenez le débit à un niveau aussi faible que possible, sans pour autant entraîner un retard inacceptable dans l’acheminement de l’échantillon vers l’analyseur. Il est préférable de commencer avec un débit faible en essayant de l’augmenter, plutôt que de commencer d’emblée avec un débit élevé.
Pour obtenir des renseignements supplémentaires sur l’utilisation des courbes de pression de vapeur d’un diagramme de phases dans le domaine de l’instrumentation analytique et des systèmes d’échantillonnage, prenez contact avec votre centre de vente et de services Swagelok.
Articles Liés
Comment positionner les buses dans votre système d'échantillonnage de liquides et de gaz naturels
Découvrez pourquoi le positionnement de la buse est crucial dans les systèmes d'échantillonnage de GNL. Apprenez les meilleures pratiques pour garantir des échantillons précis et représentatifs, et éviter ainsi des erreurs coûteuses dans votre processus d'analyse du gaz naturel.

Comment gérer la vaporisation dans les systèmes d'échantillonnage
Découvrez comment prévenir la fractionation et obtenir des résultats précis lors de la conversion d'échantillons liquides en phase vapeur au sein de systèmes analytiques. Ce guide présente les principes fondamentaux de la vaporisation, les variables clés ainsi que les meilleures pratiques pour garantir la fiabilité des performances d'échantillonnage.

10 conseils pour améliorer les systèmes d’échantillonnage
Améliorez les performances de votre système d'échantillonnage grâce à ces dix conseils pratiques. Découvrez comment réduire les erreurs, accroître la précision et garantir la fiabilité de votre processus — tout en économisant du temps et des ressources.

